
今回は有害事象と副作用の関係について学習しましょう。
「関係について学習する」とは、有害事象と副作用がどのような位置関係にあるかということを学ぶことです。
このように位置関係を学ぶのにもっともわかりやすい方法は関係を図式化することです。
以下に有害事象と副作用を図式化したものを記載します。
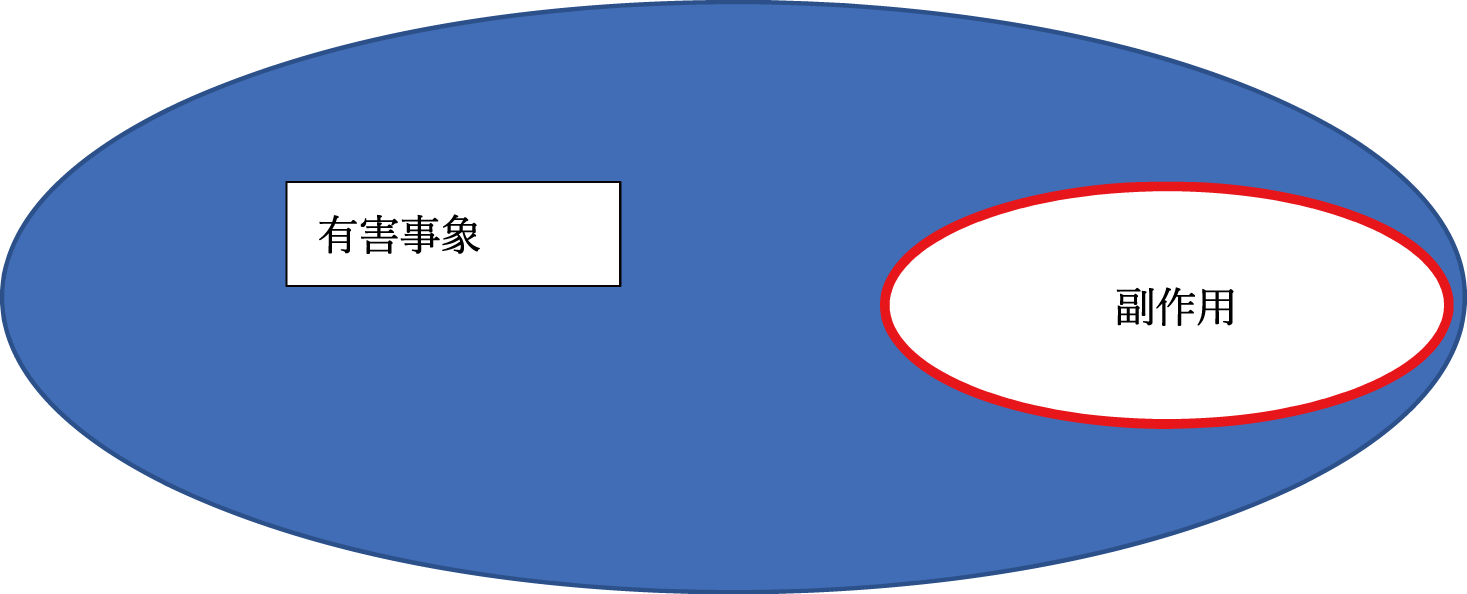
上図から判断できるように、「副作用」は「有害事象」を構成している一部分になっております。言葉で表すと次のようになります。
副作用は有害事象に含まれる。
では、「副作用」と判断されるにはどのようなことが必要でしょうか。
このことを説明する前に、「有害事象」をもう一度おさらいしましょう。
| CH E2A (治験中の安全性)より引用
有害事象(Adverse Event(or Experience) 医薬品が投与された患者または被験者に生じたあらゆる好ましくない医療上のできごと。必ずしも当該医薬品の投与との因果関係が明らかなもののみを示すものではない。 つまり有害事象とは,医薬品が投与された際に起こる,あらゆる好ましくない,あるいは意図しない徴侯 (臨床検査値の異常を含む),症状,または病気のことであり,当該医薬品との因果関係の有無は問わない。 |
ICH E2Aの定義によれば、「医薬品が投与された患者または被験者に生じたあらゆる好ましくない医療上のできごと。必ずしも当該医薬品の投与との因果関係が明らかなもののみを示すものではない。」となっており、「有害事象」は医薬品が投与された後におきる出来事となっております。また、因果関係を考えないということも読み取れます。
どうも、この「因果関係」というのが、「副作用」を説明するキーワードみたいです。
では、ICH E2Aではどのように「副作用」」を定義しているかを見ていきましょう。
| 英語
2.Adverse Drug Reaction (ADR) In the pre-approval clinical experience with a new medicinal product or its new usages, particularly as the therapeutic dose(s) may not be established: all noxious and unintended responses to a medicinal product related to any dose should be considered adverse drug reactions. The phrase “responses to a medicinal products” means that a causal relationship between a medicinal product and an adverse event is at least a reasonable possibility, i.e., the relationship cannot be ruled out. Regarding marketed medicinal products, a well-accepted definition of an adverse drug reaction in the post-marketing setting is found in WHO Technical Report 498 [1972] and reads as follows: A response to a drug which is noxious and unintended and which occurs at doses normally used in man for prophylaxis, diagnosis, or therapy of disease or for modification of physiological function. The old term “side effect” has been used in various ways in the past, usually to describe negative (unfavourable) effects, but also positive (favourable) effects. It is recommended that this term no longer be used and particularly should not be regarded as synonymous with adverse event or adverse reaction. *注記 上記の英文はICH E2Aよりそのまま引用しました。表現の不備は記載のままです。 日本語 (2)副作用(Adverse Drug Reaction) 病気の予防,診断もしくは治療,または生理機能を変える目的で投与された(投与量にかかわらない)医薬品に対する反応のうち,有害で意図しないもの。 |
上記の文章から、「副作用」とは、「投与された医薬品に対する反応のうち、有害で意図しないもの」と読み取れます。
日本語の説明よりも、英語の説明の方が詳しく、英語の次の説明から:
The phrase “responses to a medicinal products” means that a causal relationship between a medicinal product and an adverse event is at least a reasonable possibility, i.e., the relationship cannot be ruled out.
副作用とは、「因果関係」を否定できないもの、と理解できます。
また後半の文章では、昔から「side effect」という言葉があり、それが使用されてきていましたが、この「side effect」という言葉は、悪い意味(好まない作用)でも、良い意味(好む作用)でも使用するので、今後は使用しないでください、「adverse event」とか「adverse reaction」とは同義ではないですと、はっきり記載されてます。
皆さん、安全性のお仕事には、「side effect」とは使用しないようにしましょう。
さらに、英語の本文には「adverse drug reaction」と「adverse reaction」が同じ意味で使用されております。どちらの表記も可能であることが理解できます。
英語のタイトルに記載されているように、略語は「ADR」となります。
では、実際の安全性情報の業務ではどうなっているのでしょうか?
「副作用」は、有害事象の内、因果関係を否定できない事象であり、因果関係が不明も「副作用」として扱っています。
よく新聞、テレビなどのマスコミ報道で「XXX薬で副作用がおきました」というのがあります。これで、どのような内容が報道されるか理解できましたね。
次回は予測できない副作用を学びましょう。
